编者按:2026年3月27日至28日,“第九届北京血栓与止血会议暨第七届北京血液肿瘤与免疫高峰论坛”在北京隆重召开,汇聚了国内外顶尖学者、临床专家与行业领袖,齐聚一堂、共襄学术盛举,共探血栓与止血、血液肿瘤与免疫领域的前沿动态,擘画学科发展的未来蓝图,推动领域内学术交流与技术创新迈向新高度。在阵发性睡眠性血红蛋白尿症(PNH)血栓的防治方面,本次会议上,天津医科大学总医院血液内科付蓉教授进行了精彩的讲解,本文基于天津医科大学总医院及国内外多项研究数据,系统梳理了PNH血栓的流行病学特征、机制研究进展、风险预测模型及临床管理策略,以期为临床医生提供实用参考。

PNH血栓:高发病率、临床特征及影响因素
阵发性睡眠性血红蛋白尿症(PNH)是一种罕见的、由PIG-A基因在造血干细胞水平发生体细胞突变而导致的一种罕见的后天获得性溶血性疾病,临床上以血管内溶血、骨髓衰竭和血栓高发为特征。值得注意的是,血栓不仅是PNH患者最常见的并发症,更是其致残与致死的主要原因。
01、PNH血栓发病率高,显著增加致残致死风险
PNH患者发生血栓的风险是普通人群的62倍,血栓事件是PNH患者最常见并发症,数据显示29~44%的PNH患者至少发生过一次血栓事件。根据国际PNH注册处数据显示,在4134例未接受依库珠单抗治疗的PNH患者中,主要不良血管事件(MAVEs)发生率为 18.8%;血栓事件(TEs)发生率为 13.3%。
血栓毫无疑问增加了PNH患者的死亡风险,是患者致残和致死的主要原因,占已知原因死亡的40~67%。Socie G教授等在Lancet期刊上的一项研究显示, PNH合并血栓患者的标准化死亡比(SMR)高达 13.9,4年生存率仅为 40%(详见下图1)。
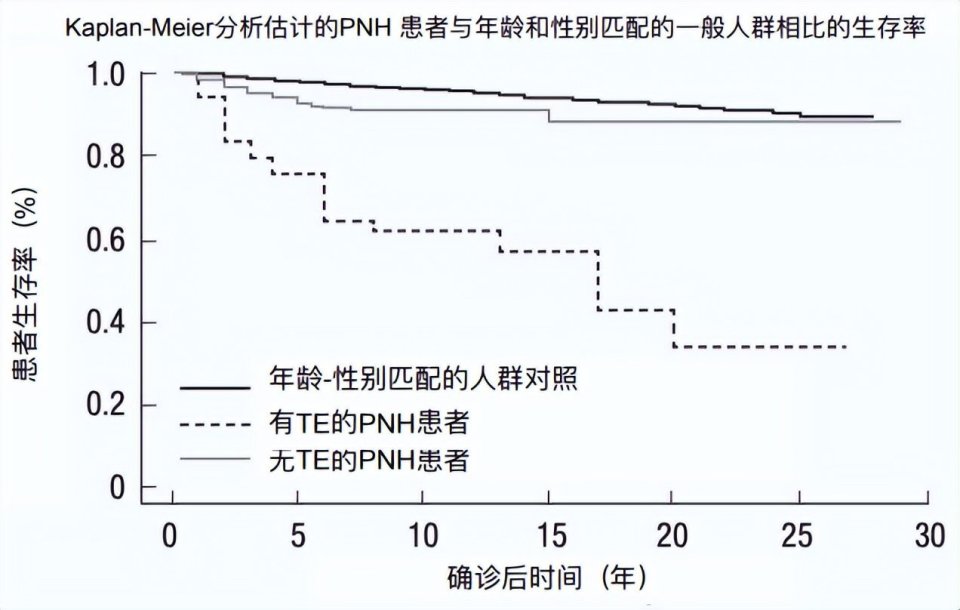
图1
中国PNH登记系统(631例)显示,血栓发生率为 8.9%(6.4/100病人年),明显低于西方国家的32.5%和韩国的18%,但近一半患者在首次血栓后会发生二次血栓。另外,2016年一项中欧美对比研究显示:亚洲患者血栓发生率 11.5%,欧美为 32.5%;亚洲患者动脉血栓比例较高(23.0% vs 1.1%),欧美则以腹部静脉血栓为主(50.5% vs 35.1%)欧美主要死亡原因为血栓(43.7%),亚洲为严重感染(40.2%)
上述研究数据表明,中国PNH患者血栓发生率虽低于欧美,但复发率高、隐匿性强,临床需高度警惕。
02、PNH血栓临床特征及影响因素研究
天津医科大学总医院通过对2014-2024年间收治的220例PNH患者进行分析,其中血栓发生率为19.09%,并将34项临床指标纳入LASSO回归分析,并进行多因素逐步Logistic回归分析,结果发现,ALB、FIB、D-二聚体、红细胞II型克隆、PNH粒细胞克隆、糖皮质激素使用及MUC4突变为PNH血栓的危险因素。
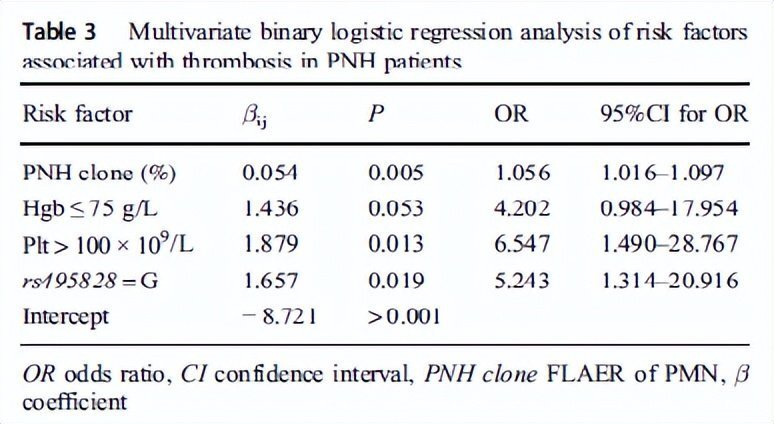
此外,142例回顾性分析证实PNH克隆大小、血小板>100×10⁹/L及ABO基因位点rs495828=G是静脉血栓的独立危险因素。
一项来自韩国的研究表明,LDH≥1.5倍正常上限与PNH血栓及死亡风险显著相关(P=0.001),而血红蛋白水平对血栓无预测价值(见下图2)。
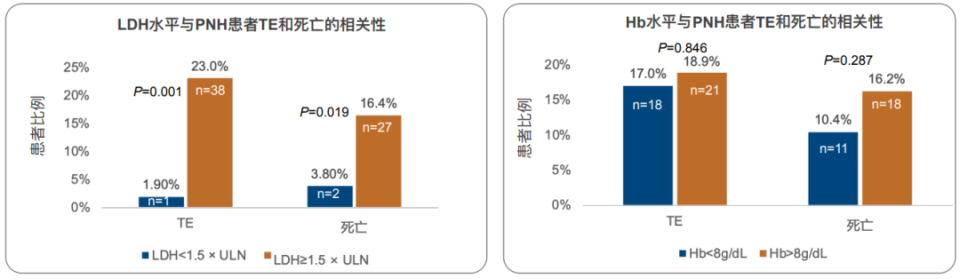
图2
综上,PNH血栓的预测因素包括PNH克隆大小、LDH水平、年龄、妊娠、糖皮质激素使用及MUC4等基因突变。
PNH血栓发病机制研究
PNH患者血栓事件的发病机制复杂,涉及多种因素的协同作用。主要包括补体系统异常激活、血管内溶血、一氧化氮生物利用度降低、血小板与中性粒细胞活化,以及凝血级联反应、补体系统和炎症细胞因子之间形成的恶性循环。
01、补体系统与溶血的驱动作用
补体系统的异常激活是PNH血栓形成的始动环节。由于造血干细胞PIG-A基因突变导致GPI锚定蛋白缺失,细胞表面缺乏CD55和CD59等补体调节蛋白,使红细胞和血小板更易受到补体攻击。C5b-9膜攻击复合物在血小板表面沉积后,可形成孔洞促使血小板内α颗粒与膜融合,释放血小板微粒体,导致血小板活化并大量产生凝血酶,显著增加血栓风险。此外,血管内溶血导致游离血红蛋白释放,消耗一氧化氮,引起血管收缩、血小板聚集和内皮功能障碍,进一步推动血栓形成(见下图3)。
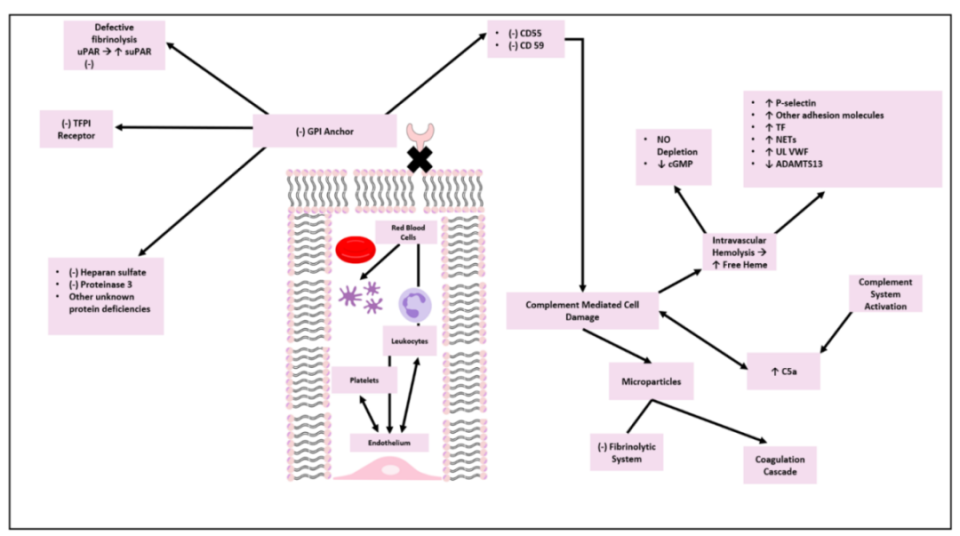
图3
02、MUC4基因突变促进终末补体沉积
通过全外显子测序和基因芯片技术,天津医科大学总医院的研究团队首次系统揭示了MUC4基因突变在PNH血栓中的重要作用。在45例经典型PNH患者中,血栓组MUC4突变率高达68.8%,非血栓组仅10.3%,MUC4突变是独立危险因素(OR=19.589,下图4)。
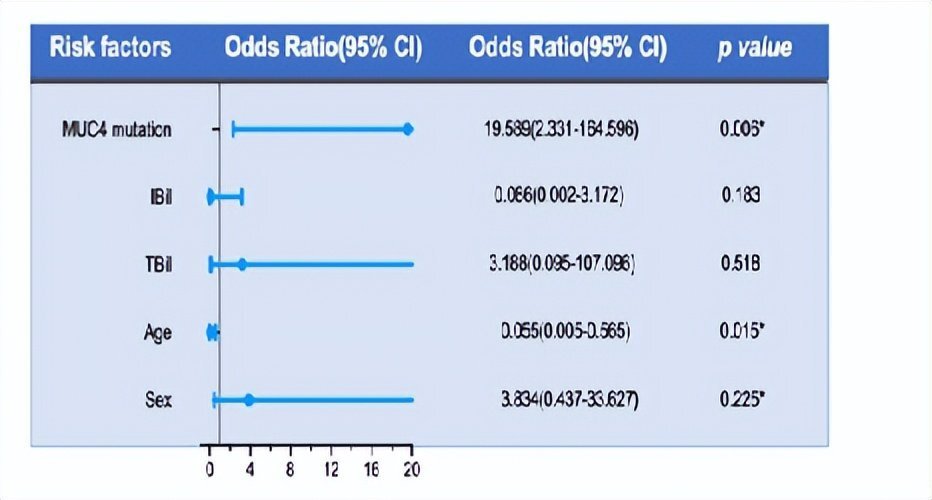
图4
机制研究证实,MUC4突变可促进终末补体C5b-9的沉积:Piga/Muc4双敲小鼠下肢深静脉血栓模型中,双敲小鼠血栓长度显著增加,血栓局部组织C5b-9沉积明显增多;细胞实验中敲低MUC4表达后,细胞表面C5b-9沉积亦增加。这些结果证实,MUC4突变通过增加终末补体沉积,促进PNH小鼠的血栓表型。
03、多组学分析揭示血小板与凝血级联激活
对PNH合并急性血栓患者进行全外显子测序、单细胞转录组测序及血浆蛋白质组学分析,从多层面揭示了血栓形成的分子基础。全外显子测序发现14个突变基因富集于细胞骨架、细胞黏附、白细胞和血小板激活通路;细胞外基质受体互作和⽩细胞经内⽪迁移相关通路。
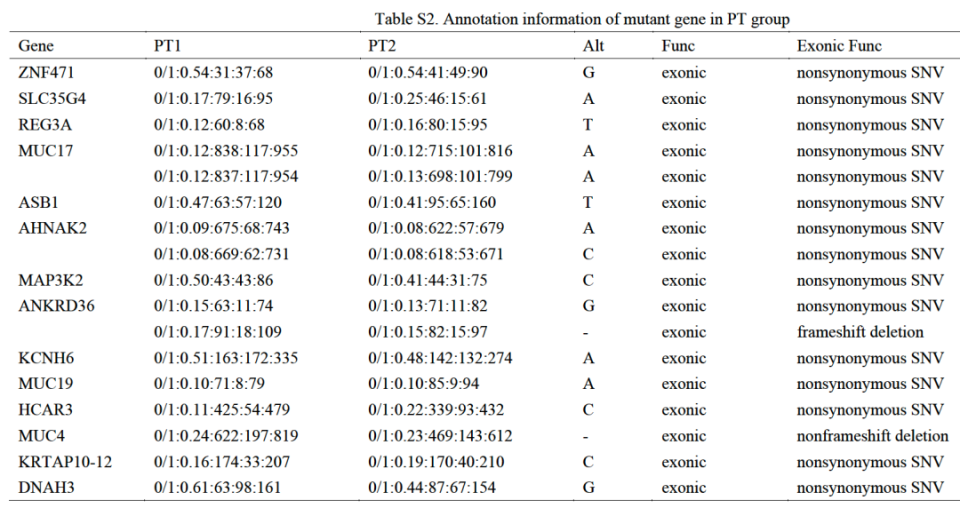
多组学分析一致证明,血小板激活、凝血级联、白细胞黏附在基因、转录和蛋白层面共同促进PNH血栓形成。
04、中性粒细胞外陷阱的“预活化”机制
研究发现,PNH患者的中性粒细胞处于独特的“预活化”状态。在无外界刺激时,其NETs形成率和游离DNA释放量已显著高于健康对照;经PMA、C3a、C5a、G-CSF等诱导剂刺激后,NETs形成反应更为强烈。血清中NETs核心标志物MPO-DNA和CitH3水平显著升高,且与血栓事件呈正相关。进一步研究表明,PNH中性粒细胞的固有特性与血浆微环境异常可协同促进NETs释放,而NETs可诱导vWF裂解位点氧化,阻止其被ADAMTS13蛋白水解,导致vWF/ADAMTS13轴失衡,促进血栓形成。
05、间接锚链蛋白PR3的作用
PNH患者中性粒细胞膜上间接锚链蛋白PR3表达降低,血浆中含量亦减少。PR3本可灭活蛋白酶激活受体1,当PR3表达下降时,血浆血小板上PAR-1含量升高,通过与凝血酶结合引起血小板聚集,从而促进血栓事件的发生(见下图5)。这一机制揭示了GPI锚定蛋白间接缺失对血栓形成的潜在贡献。
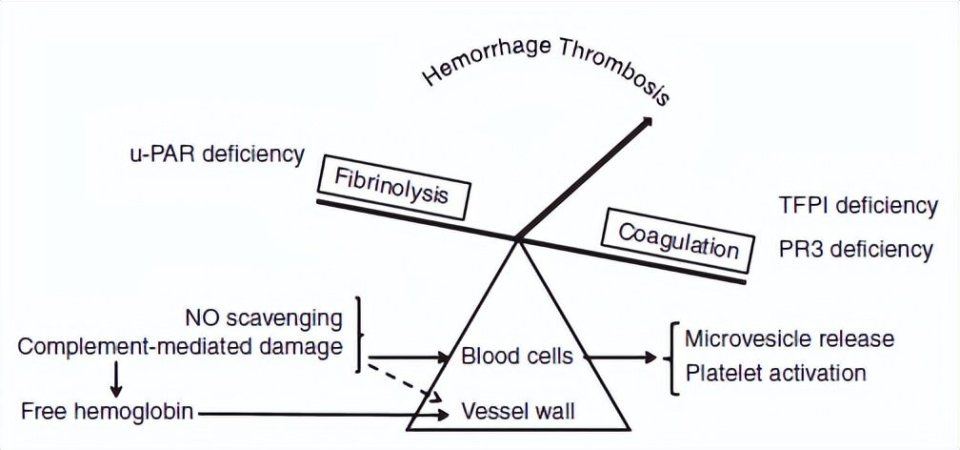
图5
PNH血栓的管理策略
01、风险预测模型的建立
天津医科大学总医院研究团队基于220例PNH患者队列(血栓发生率19.09%),通过LASSO回归和多因素Logistic分析,筛选出血清白蛋白、纤维蛋白原、D-二聚体、CD55/59- II型红细胞克隆、CD55/59- 粒细胞克隆、糖皮质激素使用及MUC4基因突变为最佳预测因素(下图6)。构建的列线图模型区分度优异(AUC=0.946),校准度良好(P=0.688),可用于个体化识别PNH血栓高危患者。
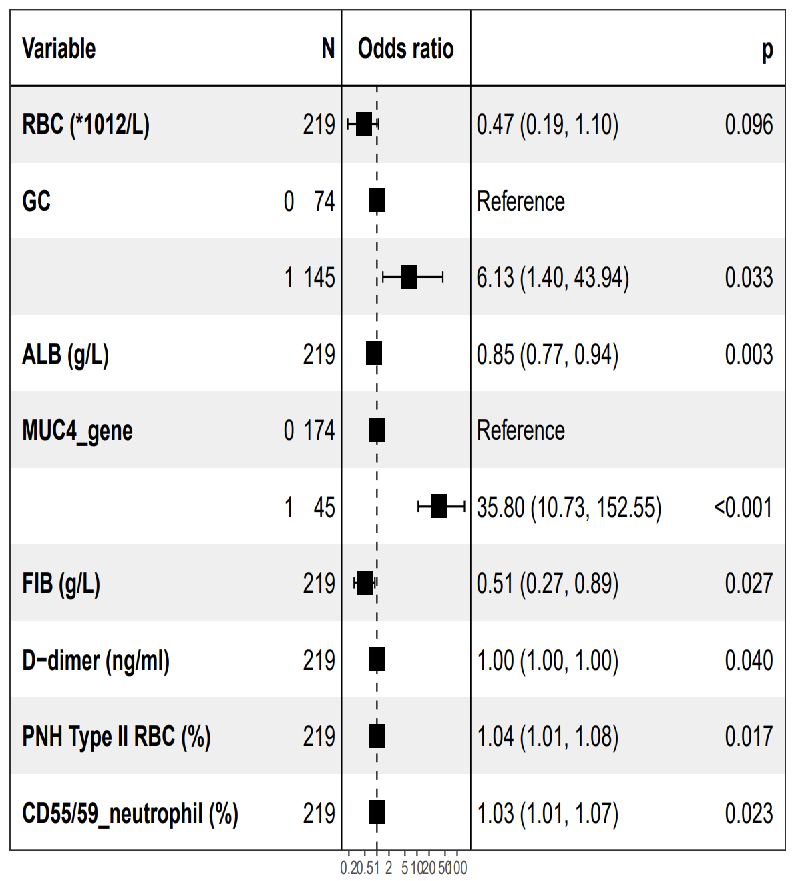
图6
此外,国际研究证实PNH粒细胞克隆>50%者10年血栓风险达44%,LDH≥1.5倍正常上限是评估血栓风险的最佳临界值(OR=7.0)。
02、抗凝治疗的策略与选择
急性血栓事件应同时启动抗凝和补体抑制剂治疗,稳定后(LDH<1.5倍正常上限)可考虑停用抗凝。对于补体抑制剂不可及的高危患者,可酌情使用抗凝药物进行一级预防;有血栓史者推荐补体抑制剂联合抗凝二级预防。
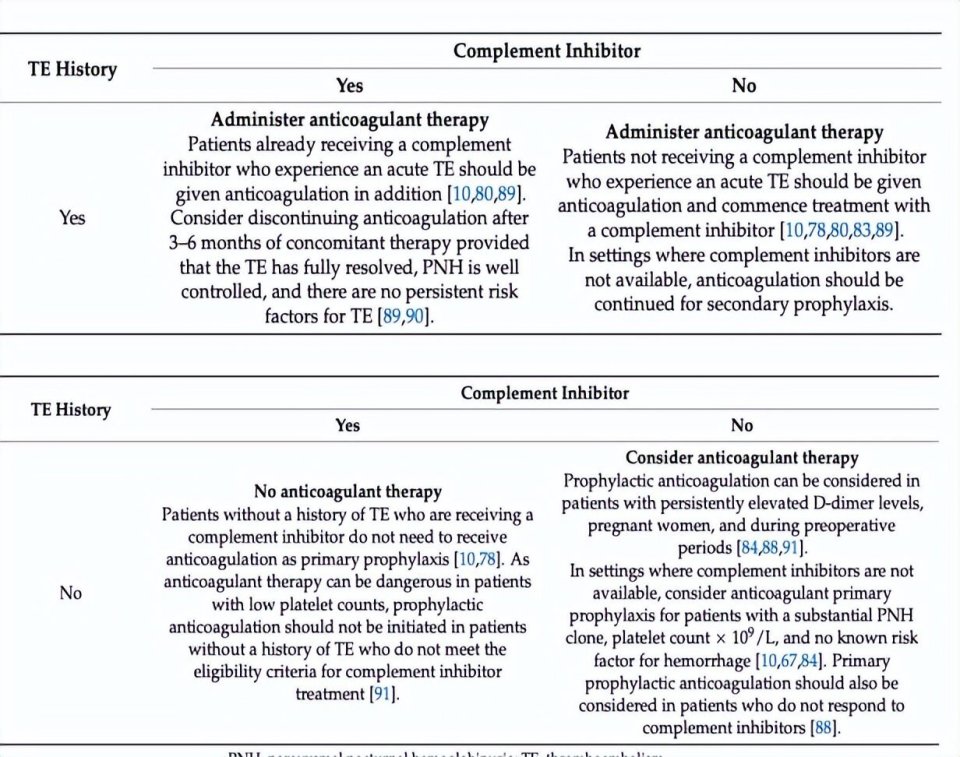
图7
在抗凝药物选择中,通常有华法林、肝素类药物以及直接口服抗凝药(DOAC),其中低分子肝素出血风险较低,直接口服抗凝药(DOAC)显示出良好安全性与有效性。英国单中心数据显示,DOAC治疗221.5患者年无血栓事件发生,致命性出血发生率仅0.11/100患者年。
03、补体抑制剂的核心治疗地位
补体抑制剂是唯一证实可预防PNH血栓的干预措施。目前常用的补体抑制剂有依库珠单抗、瑞利珠单抗、Iptacopan及Pegcetacoplan。
根据研究数据显示,依库珠单抗治疗1年内血栓事件减少92%,3年随访显示血栓发生率从11.13/100患者年降至2.14/100患者年(下降81.8%)。
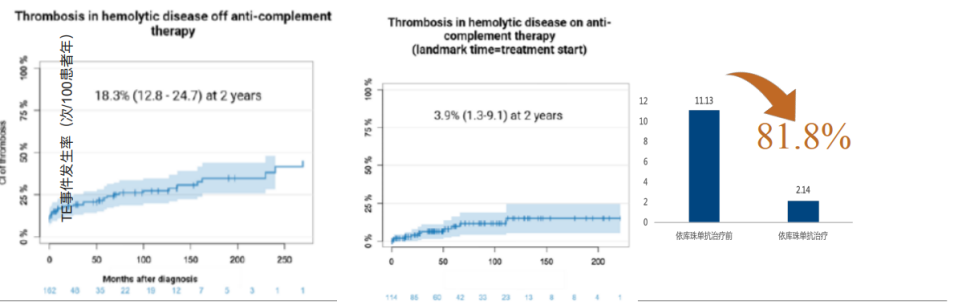
图8
另外,国际PNH登记研究证实,接受依库珠单抗治疗后血栓发生率为1.07件/100患者年,血栓风险相对降低85%(P<0.001)。
总而言之,在补体抑制剂是PNH血栓管理的基石,联合抗凝用于二级预防安全有效;DOAC显示出良好前景。
总 结
应重视PNH合并血栓,提高认识并加强临床识别 ;
PNH血栓机制主要包括:血管内溶血、血小板功能异常、NO过多消耗而合成不足、炎症介质损伤内皮系统、中性粒细胞激活、PR3表达降低致血小板聚集、纤溶系统功能障碍 ;
PNH血栓形成的影响因素:克隆大小、溶血程度、遗传背景、治疗药物等 ;
补体抑制剂和必要的抗凝治疗在PNH患者血栓管理中发挥重要作用。
专家简介

付蓉 教授
天津医科大学总医院
医学博士、主任医师、二级教授、博士生导师
天津医科大学总医院 副院长、血液病中心 主任
天津市骨髓衰竭重点实验室 主任
天津市血液病研究所 所长
天津医科大学血液病学系 主任
中华医学会血液学分会 常委
中华医学会血液学分会红细胞学组 组长
中国医师协会血液科医师分会 常委
中国医师协会血液科定考工作委员会 副主委
天津市医学会血液学分会 主委
天津市医师协会血液科医师分会 副会长
天津市医疗健康学会血液病学专业委员会 主任委员
Journal of clinical Laboratory Analysis (SCI)主编;中华血液学杂志 副总编
首届天津名医、天津市教学名师、天津科普大使、津门医学英才、天津市青年科技奖获得者、天津市高校领军人才
主持国家级及省部级课题20项,以第一完成人获天津市科技进步一等奖、天津市科技进步二等奖、中国抗癌协会二等奖、天津市抗癌学会一等奖