近期,美国国家综合癌症网络(NCCN)正式发布2026.V1版《NCCN临床实践指南:B细胞淋巴瘤》。该指南针对滤泡性淋巴瘤(FL)、边缘区淋巴瘤(MZL)、套细胞淋巴瘤(MCL)、弥漫性大B细胞淋巴瘤(DLBCL)等常见B细胞淋巴瘤的治疗方案进行了多项细节修订。本文将对其中核心更新内容进行系统梳理,为临床实践提供参考。

01
滤泡性淋巴瘤(FL)
1、检查项目
-
必要项:计划进行治疗时,需行PET/CT扫描(首选)或诊断级别的胸部/腹部/盆腔(C/A/P)增强CT;
-
适用于特定患者:血清蛋白电泳(SPEP)联合血清免疫固定电泳(SIFE)和/或免疫球蛋白(Ig)水平定量测定。
-
如计划对I、II期疾病进行放疗(RT),应行PET/CT扫描。
-
原“必要项”调整:骨髓活检+骨髓抽吸(若计划行受累部位放疗[ISRT],则用于证实临床I~II期疾病;或用于评估原因不明的血细胞减少)。
2、治疗路径
3、一线治疗方案

4、二线治疗
-
新增治疗方案:来那度胺+利妥昔单抗+艾可瑞妥单抗(1类推荐)。
-
推荐等级调整:“来那度胺+利妥昔单抗+坦昔妥单抗”从2A类推荐提升至1类推荐。
-
方案优先级调整:“来那度胺+利妥昔单抗”从首选方案调整为其他推荐方案。
-
老年或体弱患者的二线治疗中,移除“环磷酰胺±利妥昔单抗”方案。

5、三线及后续治疗
现有治疗方案基础上,修订两项脚注内容:
02
边缘区淋巴瘤(MZL)
1、一线治疗
-
首选方案分类优化:将患者明确分为“淋巴结边缘区淋巴瘤(NMZL)”和“脾边缘区淋巴瘤(SMZL)”,分别制定对应首选方案。
-
推荐等级调整:其他推荐方案中,“来那度胺+利妥昔单抗”用于NMZL的推荐等级从2B类提升至2A类。
-
老年/体弱患者一线治疗新增:针对局部疾病行ISRT作为首选方案之一。

2、二线及后续治疗

3、三线及后续治疗
-
新增首选方案:靶向CD19的Lisocabtagene maraleucel(liso-cel),适用于既往未使用过该疗法的患者(2A类推荐)。
-
方案优先级调整:将“阿基仑赛”从首选方案调整为其他推荐方案。
-
新增脚注d:若绝对淋巴细胞计数(ALC)>25000mcL,可采取两项措施:(1)考虑采用利妥昔单抗分次给药方案,第1天给予100mg固定剂量,第2天按375mg/m²给予剩余剂量;(2)考虑在利妥昔单抗给药前额外给予糖皮质激素预处理(输液前一天睡前50mg、输液当日早晨50mg、输注前即刻50mg),以降低输液相关反应发生率。
-
新增脚注h:临床条件允许的情况下,在启动抗CD19 CAR-T细胞治疗前需重复活检以确认抗原表达。

4、放疗
-
结外边缘区淋巴瘤(EMZL)患者:采用24Gy/16次(1.5Gy/次)方案,以最大程度降低急性胃肠道毒性;部分患者需追加20Gy剂量并进行密切随访。眼眶及唾液腺MZL患者可考虑4Gy/2次方案作为24Gy方案的替代选择。
-
常规方案:24Gy(局部控制率>95%)。
-
剂量调整方案:初始给予4Gy(局部控制率60%~80%),应答不佳或复发患者序贯20~24Gy。其中,眼眶MZL患者首选此方案以降低干眼症风险(已获前瞻性研究支持);腮腺MZL患者强烈推荐此方案以降低长期口干风险。其他部位MZL可结合患者偏好、放疗部位依赖性风险、患者年龄、随访依从性等因素综合选择治疗方案,并加强全程监测。
03
套细胞淋巴瘤(MCL)
1、治疗路径
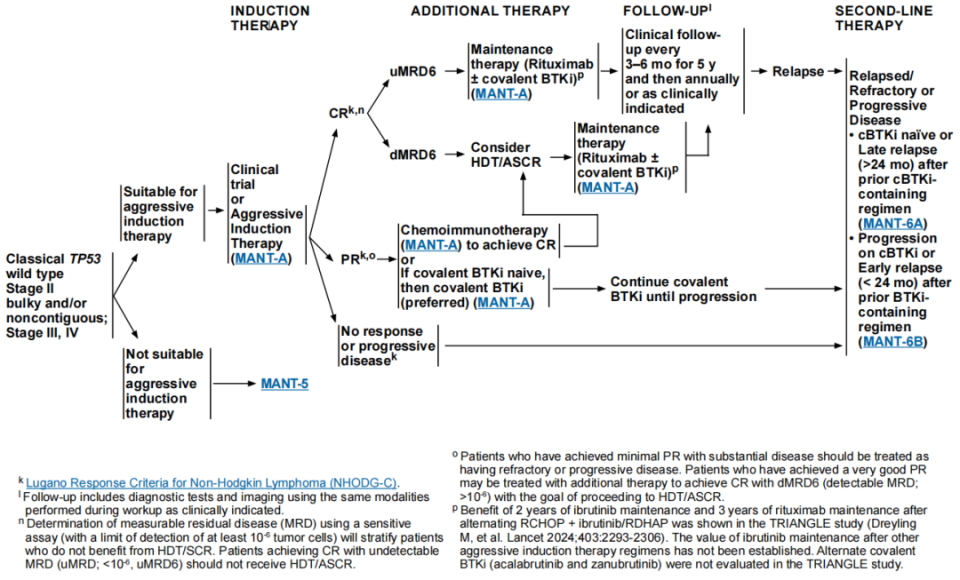
对于经典TP53野生型II期伴大肿块(非连续)、III期、IV期患者,强化诱导治疗后新增以下内容:
-
无法检测到微小残留病(uMRD6)的患者,接受“利妥昔单抗维持治疗±共价BTK抑制剂”。
-
考虑行高剂量化疗联合自体干细胞挽救治疗(HDT/ASCR)的可检测到微小残留病(dMRD6)患者,术后接受“利妥昔单抗维持治疗±共价BTK抑制剂”。
-
脚注o修订:对于仅达到轻微PR但仍存在明显病灶的患者,按难治性或进展性疾病处理;对于达到非常好的PR患者,可考虑额外治疗,目标是后续进入HDT/ASCR治疗阶段。
-
脚注p修订:交替使用R-CHOP+伊布替尼/R-DHAP方案治疗后,行2年伊布替尼维持治疗联合3年利妥昔单抗维持治疗的获益,已在TRIANGLE研究中得到证实。
2、诱导治疗
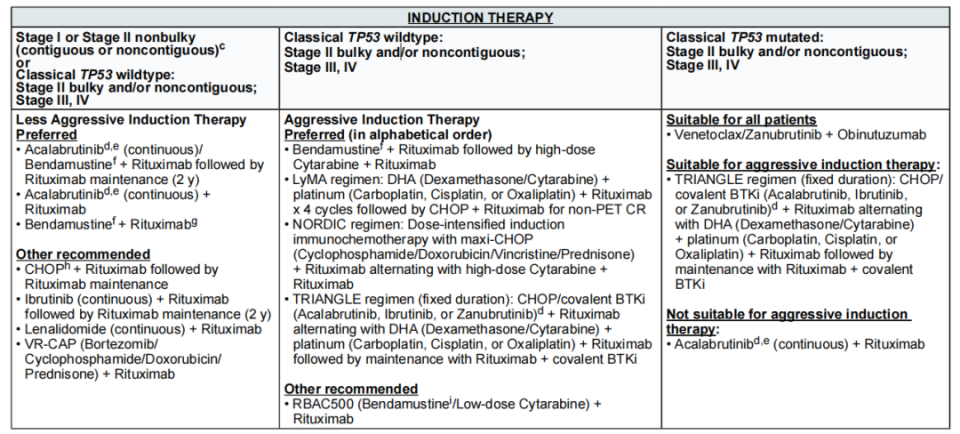
1. I期或II期伴大肿块(连续或非连续),或经典TP53野生型II期伴大肿块(非连续)、III期、IV期
-
修订首选方案:阿可替尼(持续给药)/苯达莫司汀+利妥昔单抗,序贯利妥昔单抗维持治疗(2年)。
-
方案优先级调整:将“阿可替尼(持续给药)+利妥昔单抗”从其他推荐方案提升至首选方案。
-
其他推荐方案新增:伊布替尼(持续给药)+利妥昔单抗,序贯利妥昔单抗维持治疗(2年)(2A类推荐)。
-
方案优先级调整:将“CHOP+利妥昔单抗,序贯利妥昔单抗维持治疗”“来那度胺(持续给药)+利妥昔单抗”和“VR-CAP方案”从首选方案调整至其他推荐方案。
2. 经典TP53野生型II期伴大肿块(非连续)、III期、IV期
3. 经典TP53突变型II期伴大肿块(非连续)、III期、IV期
3、维持治疗
1. HDT/ASCR或强化诱导治疗后
2. 较温和的诱导治疗后
4、二线及后续治疗
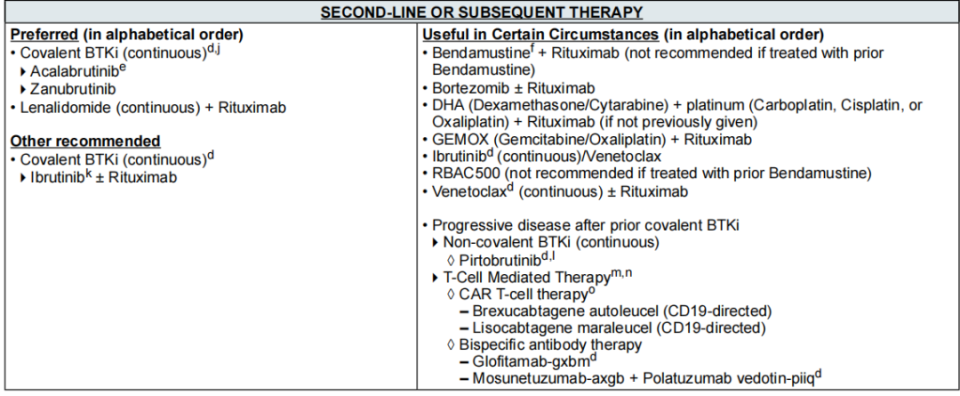
针对既往接受共价BTK抑制剂治疗后疾病进展的患者,调整如下:
-
新增治疗方案:莫妥珠单抗+维泊妥珠单抗(2A类推荐)。
-
格菲妥单抗调整:删除原限定条件“CAR-T细胞疗法和匹妥布替尼治疗后疾病进展或不适合CAR-T细胞疗法”,同时将推荐等级从2B类提升至2A类。
-
新增脚注o:特定情况下,疾病进展时可选用替代CAR-T细胞疗法。
5、放疗
-
初始治疗(不联合化免治疗):剂量由36Gy修改为24~36Gy。
-
化免治疗后巩固治疗(达到PR的患者):剂量由36Gy修改为24~36Gy。
-
化免治疗后巩固治疗(达到完全缓解[CR]的患者):剂量调整为DLBCL/高级别B细胞淋巴瘤(HGBL)20Gy,纵隔灰区淋巴瘤(MGZL)/浆母细胞性淋巴瘤(PBL)/原发纵隔大B细胞淋巴瘤(PMBL)30~36Gy。
-
新增脚注b:胃部EMZL常采用1.5Gy/次的分割剂量,以减少急性胃肠道毒性。
-
新增脚注c:相关治疗方案的中位随访时间为2~3年。
04
弥漫性大B细胞淋巴瘤(DLBCL)
1、一线治疗(伴随中枢神经系统[CNS]疾病患者)
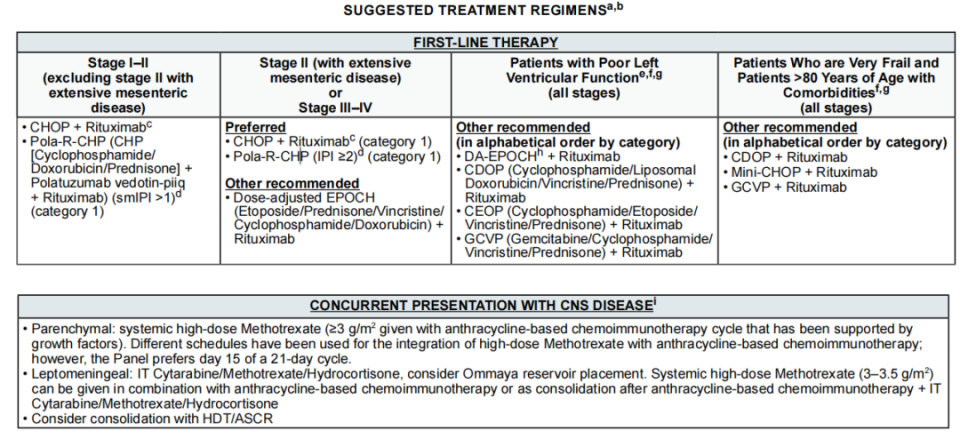
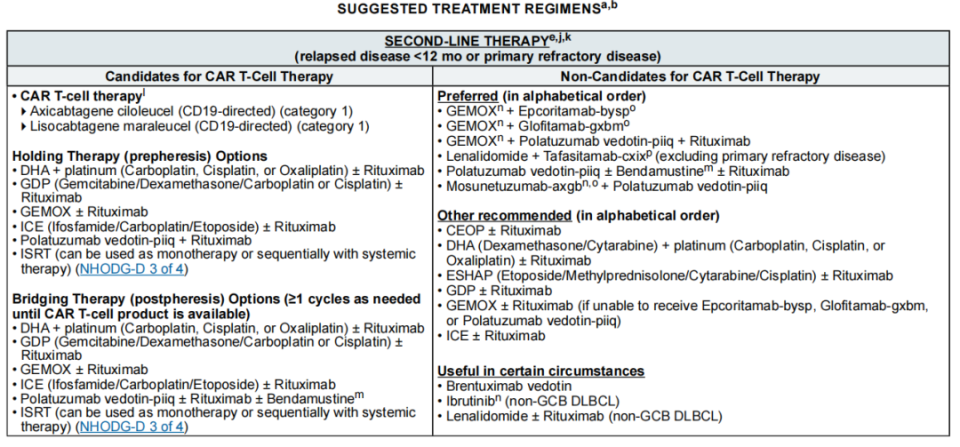
2、二线治疗
1.疾病复发持续时间<12个月或为原发性难治性疾病
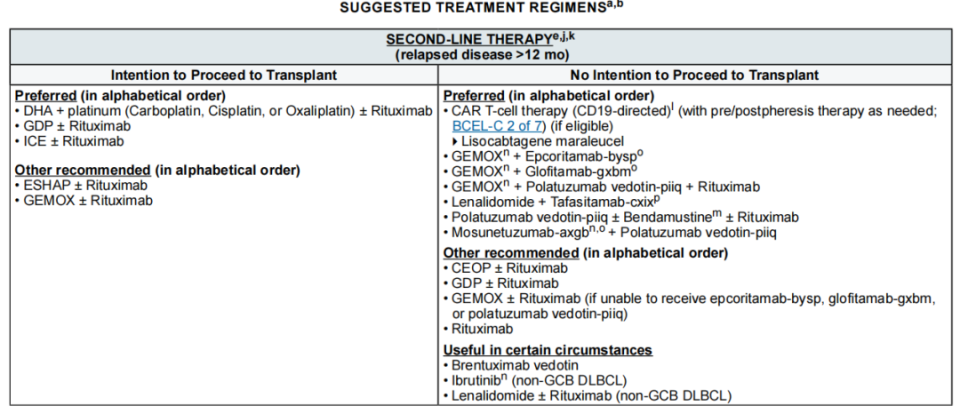
2.疾病复发持续时间>12个月
3、三线及后续治疗

4、ALK阳性大B细胞淋巴瘤(ALK+ LBCL)

5、原发皮肤弥漫大B细胞淋巴瘤,腿型(PCLBCL-LT)