慢性移植物抗宿主病(cGVHD)这一由免疫炎症驱动、以组织纤维化为核心病理特征的慢性系统性疾病,严重影响患者的生活质量。贝舒地尔作为一种口服高选择性ROCK2抑制剂,通过独特的双重机制——同时调控免疫炎症和预防/逆转纤维化,为cGVHD治疗提供了新思路。然而,其在真实世界临床实践中的表现,尤其是与“临床最佳可及疗法”相比究竟孰优孰劣?2025年发表于血液学权威期刊《Blood Advances》(影响因子=7.1)的ROCKreal研究,以创新的研究设计和严谨的统计方法给出了明确答案,为贝舒地尔的临床应用提供了堪比随机对照试验的高级别真实世界证据1。现将研究主要内容整理如下,并邀请陆军军医大学第二附属医院医院张曦教授和北京大学临床研究所阎小妍教授进行点评,以供读者阅读和参考。
为什么ROCKreal研究证据等级高,堪比RCT?1
真实世界研究常因设计缺陷、混杂因素干扰而备受质疑,但ROCKreal研究成功打破了这一成见。其采用目标试验模拟方法,本质是在真实世界数据中重现一个理想的随机对照试验(RCT)(图1)。目标试验模拟是一种观察性研究设计框架,通过模拟一个理想化的、假设的随机对照试验(RCT) 来利用真实世界数据进行因果推断。目标试验模拟的主要实施要点可总结为“3-7-2”,即声明因果问题、制订模拟方案和模拟目标研究3个实施步骤,纳排标准、治疗策略、干预分配、随访期、结局指标、因果比较和分析计划7个设计要素,对永恒时间偏倚和现用药者偏倚2个关键偏倚的控制2。
通过这一框架,ROCKreal研究在真实世界数据中实现了接近随机对照试验的因果推断强度——虽不等同RCT,但已是现有条件下较为严谨的疗效估计。
01
研究设计:从观察到模拟随机
理想化的目标试验是一个假设的随机对照试验,为真实世界研究设计提供了一个参考点,有助于避免观察性分析中常见的设计缺陷。研究明确定义了纳入标准(年龄≥12岁、cGVHD诊断、既往2-5线治疗失败)、治疗组(贝舒地尔 vs. BAT)、随访期(1年)、主要终点(6个月时的ORR)和次要终点(1年FFS),遵循临床试验设计逻辑。研究将现实中不可避免的事件如患者死亡、疾病复发、更换治疗方案——明确定义为治疗失败,与RCT中的复合终点理念一致,确保疗效评价的临床相关性。
02
统计方法:高级因果推断最大限度控制偏倚
-
使用靶向最大似然估计(TMLE):一种融合了机器学习与领域知识的统计方法,能够同时校正数十个潜在混杂因素(包括年龄、既往治疗线数、器官受累情况、合并症等),在纳入充分、合理的混杂因素并处理信息性失访/删失的前提下,尽量贴近随机试验下的边际(总体)因果效应估计。
-
校正三大偏倚:TMLE专门针对治疗选择偏倚(为何医生选A药而非B药)、失访偏倚(部分患者数据缺失)和混杂偏倚(影响疗效的其他因素)进行量化校正,使结果更接近“如果所有人均用贝舒地尔/均用BAT”的因果效应。
-
多重敏感性分析验证稳健性:研究进行了包括填补缺失数据、延长评估窗口、模拟未测量混杂等在内的多项敏感性分析,核心结论(贝舒地尔更优)始终保持稳定,证明了结果的可靠性。
研究共纳入196例(共358个治疗线)患者,旨在评估贝舒地尔对比BAT(芦可替尼、甲氨蝶呤、西罗莫司、霉酚酸酯、利妥昔单抗、伊布替尼等)治疗≥12岁且既往2-5线治疗失败的cGVHD患者的疗效和安全性。主要终点是6个月时的ORR(结局判定窗口期为治疗线开始后第2周至第26周,以26周前的最新缓解状态作为6个月时的评估结果。需要注意:ROCKreal 的ORR是为适配真实世界评估频率不一致而设计的复合结局,部分由医师判断或激素减量规则构成;因此它更强调临床实践可操作性,但也带来结局测量异质性),次要终点是1年无失败生存(FFS)率。更值得注意的是,贝舒地尔组的患者“起点”更差,中位年龄较BAT组更高、既往中位治疗线数更多以及芦可替尼经治的患者比例更高(表1)。面对更难治的患者,贝舒地尔疗效优势是否依然稳固?
 图1. ROCKreal研究设计
图1. ROCKreal研究设计
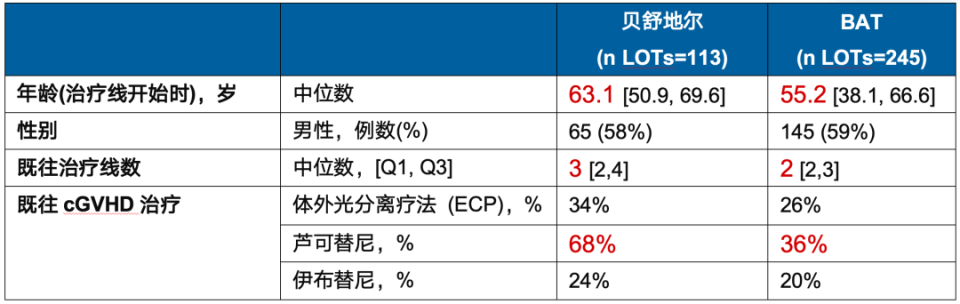 表1. 患者基线特征
表1. 患者基线特征
ROCKreal研究中贝舒地尔的疗效如何?1
ORR优异:贝舒地尔组6个月时的ORR较BAT组相对改善44.2%
与BAT相比,贝舒地尔显著改善了cGVHD患者6个月时的ORR(38.7% vs. 26.8%, 单侧P=0.031),相对改善为44.2%;缓解率的绝对增幅为11.9%(图2),即每100例患者接受贝舒地尔治疗,6个月时获得疾病缓解的患者较BAT组多12例。
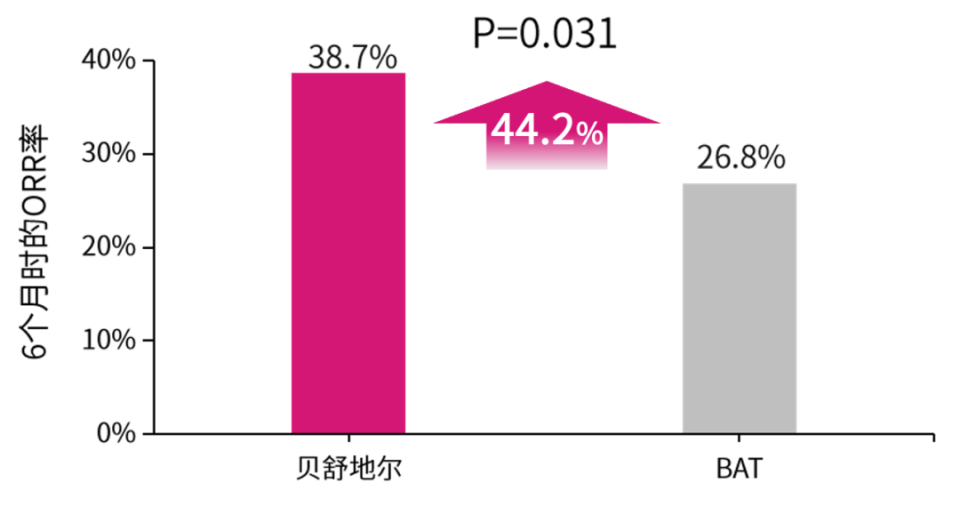 图2. 6个月时的ORR比较
图2. 6个月时的ORR比较
FFS优异:贝舒地尔组1年FFS率显著高于BAT组
与BAT相比,贝舒地尔显著改善了cGVHD患者1年FFS率(61.2% vs. 47.8%, P=0.032),两组间差异为13.5%(P=0.032)(图3),即贝舒地尔能显著降低治疗失败事件发生率。
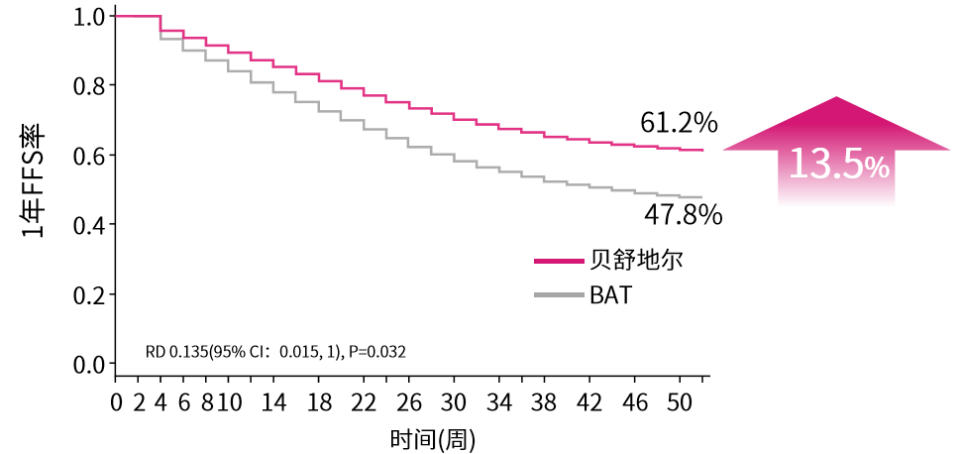 图3. 1年FFS比较
图3. 1年FFS比较
中位DOT更长:贝舒地尔组为11.3个月长于BAT组
贝舒地尔组患者中位治疗持续时间(DOT)为11.3个月,而BAT组的中位DoT仅8.5个月(图4)。
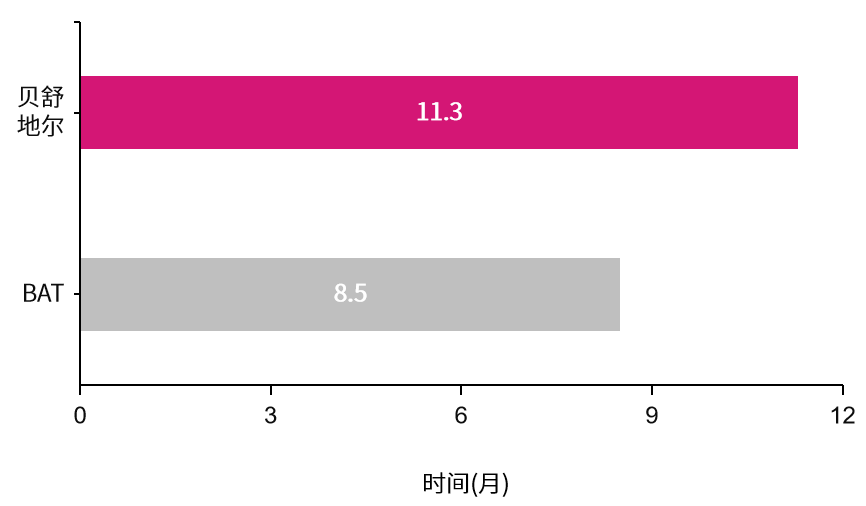 图4. 中位治疗持续时间比较
图4. 中位治疗持续时间比较
ROCKreal研究中贝舒地尔的安全性如何?
安全性分析进一步巩固了贝舒地尔的治疗价值。贝舒地尔治疗线中任何AE的发生率低于BAT组(27% vs.36%)(图5); 根据治疗线计算的每100 LOT年的AE发生率【总AE数/总暴露时间)×100】,贝舒地尔组为41.2%,BAT组为51.3%。在对AE的严重程度原因分析中,贝舒地尔组“危及生命”的AE发生率更低(2% vs.16%)。
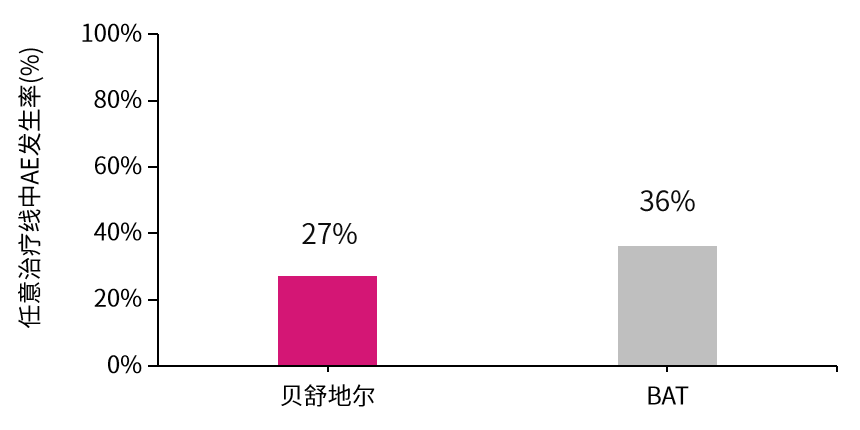 图5. 治疗线中任何AE的发生率比较
图5. 治疗线中任何AE的发生率比较
总 结
ROCKreal研究不仅仅是一项证明贝舒地尔有效的研究,它更是一次真实世界研究方法学的典范展示。通过堪比RCT的严谨设计,证实贝舒地尔治疗cGVHD的疗效显著优于最佳可及疗法,且不良事件发生率率更低。因此,本研究支持贝舒地尔作为一线治疗失败的cGVHD患者的一种有效且安全性良好的治疗选择。
张曦教授点评:贝舒地尔作为一种高选择性ROCK2抑制剂,目前被广泛用于cGVHD的治疗。ROCKstar及其随访研究证实,贝舒地尔长期治疗的中位持续缓解时间可达77周(~20个月),肿瘤复发率<3%且耐受性良好3-4。基于ROCKstar等研究结果,2025 CSCO《造血干细胞移植治疗血液系统疾病指南》推荐贝舒地尔作为cGVHD的二线治疗药物,I级推荐5。与ROCKstar研究相比,ROCKreal研究中贝舒地尔组患者芦可替尼经治比例更高,这可能意味着该组患者cGVHD疾病更晚期、应答可能性更低。此外,患者年龄也稍年长。尽管存在这些差异,贝舒地尔在ROCKreal研究中仍显示出显著的临床获益,这进一步印证了其在ROCKstar研究中观察到的疗效。
与BAT相比,贝舒地尔6个月时的ORR改善了44.2%;在改善1年FFS方面也显示出有益效果,这可能预示着更好的疾病控制。ROCKreal研究中贝舒地尔组中位治疗持续时间为11.3个月。该研究的一个重要启示在于,临床医生在cGVHD的管理过程中,应致力于确保足程治疗,以帮助患者达到并维持深度缓解。cGVHD由免疫炎症介导,是以纤维化为病理性改变的慢性系统性疾病,其长期治疗目标是建立免疫耐受,疾病症状不再复发或无明显加重6。实现这一目标并非简单地“压制”免疫系统,而是将其功能状态由“攻击”引导至“忽略”与“接受”。这种功能重塑,远比短期的炎症控制更为复杂,恢复和维持免疫稳态是一个需要长期治疗方能达成的过程。因此,临床实践中应确保足疗程治疗,避免过早停药,cGVHD的本质是一场“马拉松”而非“冲刺”。在疾病的长期管理期间,选择药物需兼顾疗效与安全性,贝舒地尔在提升缓解率、延长无失败生存的同时,展现出更优的耐受性,尤其是大幅降低了危及生命的严重事件风险,这使其成为长期管理策略中的支柱性药物。
cGVHD患者需要长期随访和规范管理,贝舒地尔凭借其抗炎和预防/逆转纤维化双重机制及良好的疗效和安全性,成为了医生和患者在漫长治疗道路上可以信赖的伙伴。
阎小妍教授点评:在观察性研究中开展因果推断,传统方法往往面临结构模糊、偏倚难控、估计不稳等多重挑战。近年来,“目标试验模拟”(Target Trial Emulation, TTE)与“靶向最大似然估计”(Targeted Maximum Likelihood Estimation, TMLE)作为两种新兴框架与方法,分别从研究设计与统计估计两个层面,为提升观察性研究的因果推断质量提供了有力支持。ROCKreal研究将这两大前沿理念与方法系统结合,是真实世界证据生成方面的一次成功实践。
目标试验模拟的核心在于以随机对照试验为蓝图,结构化地设计观察性研究。它要求研究者在分析前明确定义纳入标准、治疗策略、时间零点、随访期、结局指标等关键要素,从而在观察性数据中“模拟”出一项假设的RCT。这种设计思路的优势不仅在于提高了研究的透明度和可重复性,更在于它能有效规避常见的时间相关偏倚。ROCKreal研究采用这一国际前沿框架,目的是通过真实世界数据模拟一项假设的Ⅲ期随机对照试验。该研究预先明确定义了一个理想化的目标试验方案:纳入对2-5线治疗无效且未使用过贝舒地尔的慢性移植物抗宿主病患者,将其分为贝舒地尔组与临床最佳可及疗法组,治疗开始后随访1年,并于第6个月评估总缓解率、第1年评估无失败生存率。这一框架为观察性研究提供了类似随机对照试验的参照标准,从源头上降低了常见的时间相关偏倚(如永恒时间偏倚)。
如果说目标试验模拟是从研究架构上向金标准看齐,那么靶向最大似然估计则是从估计技术上追求稳健与效率的极致。TMLE是一种双重稳健、效率最优的估计方法,它通过巧妙的“靶向修正”步骤,确保只要倾向评分模型或结局模型中有一个设定正确,因果效应估计便是无偏的,并能达到最小的渐近方差。在ROCKreal研究中,统计分析的核心正是TMLE方法。研究团队利用TMLE同时校正了治疗选择的非随机性、信息性失访以及基线混杂因素等多重偏倚。通过融合机器学习算法与临床专家整理的混杂因素集,TMLE稳健地估计了贝舒地尔与最佳可及疗法在校正后的6个月总缓解率及其率比与率差,并构建了基于稳健标准误的置信区间。对于1年无失败生存率,同样采用TMLE进行生存分析,有效处理了基线不平衡与信息性右删失问题。此外,为验证结果的稳健性,ROCKreal研究开展了一系列严谨的诊断与敏感性分析,包括模拟未测量混杂的影响、对缺失数据进行多重插补、扩展结局评估窗口、考察时期效应等,所有分析均一致支持贝舒地尔疗效更优的核心结论。ROCKreal研究没有回避真实世界的复杂性,而是主动通过TTE框架进行结构化设计,并运用TMLE方法进行多重偏倚校正与稳健估计,从而在真实世界环境中实现了接近随机对照试验的因果推断强度。这标志着真实世界证据生成范式的一次重要升级。虽然TTE无法完全替代RCT中的随机化过程来处理未测量混杂,但ROCKreal研究通过严格的敏感性分析,在现有的真实世界数据条件下,提供了目前最为严谨的疗效估计。
专家简介

张曦 教授
陆军军医大学第二附属医院血液病医学中心主任
中国人民解放军血液病中心(军队临床重点专科)主任
主任医师、教授,博士(后)导师、长江学者特聘教授
主要从事“造血干细胞移植”的临床与基础研究,主持国家干细胞重点研发专项、国家自然科学基金重点类项目、军队课题重点项目、重庆市冲刺项目、重大课题等52项;在JCO、JHO、JAMA Oncology、Blood、Lancet Haematology、JCI、Leukemia等杂志发表SCI论文152篇,主编专著3部,副主编3部;执笔行业指南12项,参编50项;第一完成人获国家科技进步二等奖1项、中华医学科技一等奖1项、重庆市科技进步一等奖3项、二等奖1项、军队医疗/科技成果二等奖3项、中国抗癌协会科技奖三等奖1项、重庆市高等院校优秀教育科研成果三等奖1项,获批国家发明专利68项。
目前担任中华医学会血液学分会副主任委员、中国医师协会血液科医师分会常务委员、中国抗癌协会血液肿瘤专委会副主任委员、中国血液病专科联盟副理事长、中国病理生理学会实验血液学专委会常务委员、Blood & Genomics杂志主编;BMT中文版副主编;The Lancet, JHO, Nat Cell Biol, Leukemia, The Lancet Haematology, Science Bulletin, CMJ, 中华血液学杂志等杂志编委和审稿专家

阎小妍 教授
北京大学临床研究所,生物统计部主任
中国医师协会 循证医学专业委员会常务委员
中国药品监督管理研究会 药品检查与合规研究专业委员会 委员;
中国药学会 抗肿瘤药物专业委员会 委员;
中国临床肿瘤学会(CSCO)生物统计学专家委员会 委员;
中国抗癌协会 肿瘤药物临床研究专委会 委员;
参考文献
1.Hall K, Lazaryan A, Der Laan MV, et al. Blood Adv. 2025 Aug 28:bloodadvances.2025015832.
2.卢存存,等.协和医学杂志,2024,15(2):422-428.
3.Cutler C, et al. Blood. 2021 Dec 2;138(22):2278-2289.
4.Cutler C, et al. EBMT 2024. OS13-01.
5.CSCO《造血干细胞移植治疗血液系统疾病指南》2025版.
6.Flowers ME, et al. Blood. 2015;125(4):606-615.
MAT-CN-2601442/1.0/2026.2
免责声明:该信息仅作医学和科研参考,赛诺菲不建议以任何与您所在国家所批准的处方信息不符的方式使用本产品。本材料仅供医疗卫生专业人士使用。